
När du ser rubriker om en diabetesprodukt återkallar och inser att din medicinska anordning kan påverkas kan panik komma in. Vad nu?
Mot bakgrund av de senaste produktsäkerhetsnyheterna om Medtronic-insulinpumpar och Insulets Omnipod DASH-system (se detaljer nedan) började vi tänka på den händelsekedja som följer rubrikerna:
- Vad händer om kunderna är bekymrade över att fortsätta använda produkten?
- Kommunicerar företaget tydligt och tillhandahåller adekvat kundservice?
- Bryr sig sjukförsäkringsföretag om en produkt som de täcker eller rekommenderar medför möjliga faror?
- Hur svarar läkare och diabetesvårdsspecialister på patienter med oro?
Allt detta slog hemma nyligen för Paul Dobbertin, en långvarig typ 1 i förorterna i Chicago som blev orolig för sin Medtronic-insulinpump efter att ha sett en svärm av mediatäckning efter den senaste FDA-varningen om en produktåterkallelse. Han ringde företaget och kämpade för att få en ersättningsenhet, trots att kundtjänsten bagatelliserade situationen och insisterade på att hans enhet inte behövde bytas ut.
"Vi har rätt att vara oroliga", säger han. "Att hantera alla detaljer i ett system tillsammans med typ 1-diabetes är mycket arbete och dyrt redan, utan den extra oro för felaktig utrustning och ett känt problem."
Enheten påminner om: Vad du borde veta
Först bör du inte bli förvirrad av det olika språk som används i dessa situationer. Ordet ”återkallelse” betyder inte alltid att du måste returnera en produkt. Det finns också meddelanden om "korrigering", "borttagning av marknaden" och andra relaterade etiketter. Se den här guiden till FDA-definitioner av de olika fallen.
FDA förklarar att de flesta återkallelser är ”frivilliga åtgärder” som utförs av tillverkare och distributörer som en del av deras ansvar för att skydda folkhälsan när vissa produkter kan utgöra en risk för skada eller på annat sätt är defekta.
I de flesta fall påverkas endast vissa satser (specifika modeller eller SKU-nummer) av produkter. Så oftast är det en bedömning från fall till fall om en avkastning är motiverad för en viss enhet, om problemet i fråga gäller.
Här är detaljer om de senaste diabetesåterkallelserna som tillkännagavs i början av 2020:
Medtronic Minimed 600-seriens insulinpumpar: Återkallande av hållarring
Minimed 600-serien av enheter påverkas av en liten del på toppen av pumpen som kallas hållarringen, som ska hålla insulinbehållaren säker inne i pumpen. En funktionsstörning kan orsaka att den spricker eller lossnar, vilket kan störa insulinavgivningen och eventuellt leda till att en användare får mer eller mindre insulin än vad de ska. Det skulle inte leda till en tömning av behållaren, berättar Medtronic, men kan orsaka en fördröjning av insulintillförseln eller en snabbare, planerad bolus som skiljer sig från vad som förväntades.

Medtronic utfärdade ursprungligen ett brådskande säkerhetsmeddelande om denna fråga den 21 november 2019 och meddelade FDA om det. Vid den tiden arbetade företaget redan med en handlingsplan med tillsynsmyndigheter för att hantera de potentiellt felaktiga delarna av enheten.
Det är viktigt att det inte är ovanligt att en tillverkare utfärdar en säkerhetsvarning eller en anmälan och att FDA sedan utfärdar en återkallningsklassificering några månader senare. Det är vad som hände här, med FDA som utfärdade en klass 1-återkallelse den 12 februari 2020 och betecknade detta som den allvarligaste typen av återkallande av enheter som de utfärdar.
Hur många enheter påverkas?
Totalt 322 005 enheter påverkas, inklusive:
- alla partier av Minimed 630G-pumparna distribueras från september 2016 till oktober 2019
- alla delar av 670G Hybrid Closed Loop-systemet distribueras mellan juni 2017 och augusti 2019
Några skador eller dödsfall?
Enligt FDA-rapporten, baserad på företagsdata, fick Medtronic 26 421 klagomål om just detta fel i fästet, eftersom dessa insulinpumppartier distribuerades. Ingår i den informationen är 2175 ”skador” och en möjlig dödsfall relaterad till denna fråga.
Yikes! är ett första svar när man ser dessa siffror. Men samtidigt betonar Medtronic att uppgifterna kan vara vilseledande om de tas ur sitt sammanhang. Av de totala 2175 incidenter märkta "skador" som inkluderade höga eller låga glukoshändelser var 94 procent (2045 totalt) "självhjälpande av patienten och krävde ingen medicinsk intervention." När det gäller den rapporterade dödsfallet finns det inga avgörande bevis för att den var relaterad till en lös, skadad eller saknad hållarring. Men det kan inte heller uteslutas.
I vår tidigare fördjupade täckning av produktåterkallelser pratade DiabetesMine med FDA-insiders och företagstjänstemän som uppmanade försiktighet när det gäller att titta på återkallningsnummer i rätt sammanhang - särskilt eftersom FDA: s databas med "negativa händelser" är långt ifrån perfekt.
”Du kan inte bara titta på antalet återkallelser och dra slutsatser baserat på dessa siffror ensam. Du måste ta i sammanhanget vad återkallelsen var, hur den hittades och vad som hände med företaget vid den tiden. Det är svårt att göra utifrån, eftersom du inte har dessa samtal och sammanhang hela tiden, ”varnar Dr. Courtney Lias, chef för FDA: s avdelning för kemi- och toxikologiapparater.
Under tiden har vår D-gemenskap varit mättad med Medtronic säkerhetsvarningar de senaste månaderna: från FDA: s varning i mitten av november om äldre insulinpumpar och cybersäkerhet, till nyhetsrapporter om en federal rättegång inlämnad med hänvisning till en kvinna i Florida som hade dött 2 år tidigare som en möjlig biprodukt av att använda ett Minimed 530G-system som hade en återkallelse knuten till en eventuellt felaktig infusionsplats.
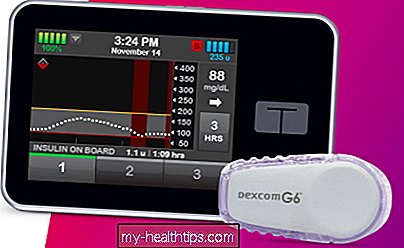
Omnipod DASH-styrenhet: Programvarufel
Inom en dag från Medtronic 600-seriens återkallande tillkännagav Insulet en korrigeringsvarning för medicintekniska produkter om den slanglösa Omnipod DASH-patchpumpen och dess personliga diabeteshanterare (PDM) som används för att kontrollera systemet. Meddelandet beskrivs som en försiktighetsåtgärd och säger att det finns en avlägsen möjlighet att PDM ”kan föreslå en insulinbolusmängd baserat på felaktig information” och det kan leda till att för mycket eller för lite insulin levereras.
Specifikt handlar frågan om bolus-kalkylatorfunktionen som används för att räkna ut mat- och korrigeringsdoser baserat på ett aktuellt blodsockervärde (BG) och användarens insulin ombord (IOB). Normalt förhindrar PDM att en avläsning äldre än 10 minuter kan användas i beräkningar. Men med denna glitch dras äldre data.
Problemet är specifikt för programversion 1.0.50 och tidigare (se Om-menyn på PDM för att ta reda på vilken version du har).
Vid tidpunkten för varningen hade 11 klagomål kommit in om denna fråga och inga skador rapporterades, enligt Insulet. Och det betyder inte att du inte kan använda DASH PDM - bara att du bör vara extra försiktig för att se till att ett aktuellt BG-värde anges när du använder bolusräknaren.
Enligt varningen utvecklas en mjukvaruuppdatering för att åtgärda problemet som är planerat att bli tillgängligt i mars 2020. Nya PDM: er med fixen kommer att skickas ut till berörda kunder, och företaget säger att de kommer att kontakta dessa kunder när det är dags att fartyg.
Trots dessa försäkringar kan naturligtvis personer med diabetes (PWD) ha kvarvarande frågor och oro.
Illinois-insulinpumper "skulle inte leva med rädslan"

Dobbertin i Illinois, för en, hade använt en Minimed insulinpump sedan mitten av 1990-talet och hade varit på 670G i ett par år. Medan han inte var helt nöjd med sin användarvänlighet totalt sett, blev kvalitetssäkring inte ett angeläget problem för honom förrän i november 2019.
Trots att han mottog en säkerhetsvarning från Medtronic och försäkrades av företaget att allt var OK, började Dobbertin oroa sig för att hans 670G-enhet skulle kunna påverkas efter att ha sett de senaste nyheterna om FDAs återkallningsmeddelande.
Han ringde Medtronics kundtjänst för mer information. Ett förinspelat meddelande beskrev återkallelsen och han fyllde i ett formulär online. Han tog av pumpen och lade den i en låda och vände sig till flera dagliga injektioner (MDI) efter behov. Efter en hel dags väntan utan svar ringde han tillbaka för att nå kundservice om vad han hade sett rapporterat.
”(Rep) beskrev de flesta nyheter som rapporterades som felaktiga och sa att pumpen faktiskt inte återkallades,” sa Dobbertin till DiabetesMine. ”Det här förvirrade mig bara mer. Nyheterna på nätet - CNN, NBC, BBC och till och med FDA - verkade alla säga något annat. Jag vet att nyheter blir vridna, men det faktum att så många hade rapporterats skadade var skrämmande. ”
Även om hans pumpdel i fråga såg intakt ut, ville Dobbertin inte riskera den. Hans vision är inte bra, och han var orolig över att behöva hålla ett öga på enheten eftersom den kan gå sönder när som helst - särskilt eftersom hans garanti redan hade upphört att gälla. Han har haft svåra insulinereaktioner med lågt blodsocker tidigare, där han har vaknat för att se sjukvårdare stå över honom, och han ville inte uppleva det igen.
"Jag uttryckte att jag bara inte skulle leva med rädslan för att av misstag överdosera mig med en enorm mängd insulin, vilket (möjligen) redan hade hänt någon på grund av en känd brist," sa han.
Trots inledande motvilja mot att byta ut pumpen skickade en handledare så småningom en ersättningsenhet inom några dagar. Dobbertin är nöjd med den service han fick i hanteringen av sitt ärende, även om hans 670G inte tycktes påverkas av denna fråga.
Han är inte ensam, eftersom Medtronic översvämmas av hundratals samtal under de första dagarna av återkallande nyheter. PWDs som delar med sig av sina erfarenheter på nätet uttrycker blandade känslor om allvaret med denna speciella återkallelse, och vissa noterar att det är "no big deal" och andra uttrycker stor oro.
New York D-Mom: 'Lucky to have dodged a bullet'

D-Mom Wanda Labrador i Rochester, New York, säger att hennes familj påverkades av denna senaste Medtronic-återkallelse, men lyckligtvis hade de slutat använda den redan innan företaget utfärdade det brådskande säkerhetsmeddelandet förra hösten.
Labradors son Justice fick diagnosen 3 år på Thanksgiving Day 2012, och att han sommar började använda en blå Minimed insulinpump efter sommaren. Så småningom, efter att ha väntat på löftet om teknik med sluten slinga, började Justice på 670G-pumpen i juli 2018.
Men inom ett par månader säger Wanda att hon märkte att hållarringen ofta skulle lossna och att hon skulle behöva dra åt den regelbundet. Det fortsatte tills det så småningom blev slitet och flisat, och på julafton 2018 ringde hon Medtronic för att rapportera skadan. De fick en ersättningspump nästa dag (God jul?). Men 5 månader senare säger hon att samma sak hände igen; hållarringen lossnade och försvann.
Många andra i chattgrupper på nätet rapporterade liknande problem och sa att de hade ringt företaget om det - ibland fått en ersättare, men ofta hörde kundtjänstrepresentanter uttrycka förvåning och då och fick veta att det inte var något att oroa sig för.
"Jag kände att något var fel med pumpen, även om Medtronic aldrig skickade en varning om faran med att ha en lös eller saknad ring", säger hon. "Det var tillfällen då hela reservoaren bara skulle glida ut ... det var inte OK!"
Bekymrad, men också för att ta en paus från själva pumpterapin, slutade Justice använda 670G och gick tillbaka på injektioner under sommarmånaderna. Han gick så småningom till diabetesläger och lärde sig om Omnipod och Dexcom, och trots att han fortfarande hade en Medtronic-pump i garantin, godkände deras försäkring de nya enheterna. Trots det är Labrador fortfarande tekniskt en Medtronic-kund i garantin men har inte fått något brev eller meddelande om detta fel på låsringen.
"När jag såg mediatäckningen kände jag mig lycklig att ha undvikit en kula och att min son aldrig skadades", säger hon. ”Samtidigt var jag upprörd över att det tog så lång tid för allmänheten att ta reda på den möjliga skada som problemet kan orsaka. Människors liv står på spel och det är inte rättvist att pumparna inte återkallades tidigare. De måste göra bättre. ”
Påverkar produktåterkallande sjukförsäkringsskyddet?
Stora försäkringsbolag som Anthem och Blue Cross Blue Shield säger att de tar hänsyn till återkallande information. Men ingen av försäkringsgivarna DiabetesMine pratade med under veckan efter de senaste diabetesåterkallelserna indikerade att de hade faktiska data tillgängliga om hur ofta säkerhetsfrågor tas upp, eller hur deras institution kan använda den informationen för att fatta täckningsbeslut.
Med Medtronic's "favoritvarumärkesavtal" med UnitedHealthcare (UHC) som begränsar medlemmarnas tillgång till icke-Medtronic-diabetesanordningar har vissa undrat om UHC tar hänsyn till denna klass I-återkallelse av sitt föredragna varumärke.
UHC: s kommunikationsdirektör Tracey Lempner säger att Medtronic underrättade försäkringsbolaget 2019 om denna fråga som påverkar Minimed 600-serien av insulinpumpar.
UHC utfärdade sedan ett uttalande till berörda medlemmar som läste: ”Säkerheten för våra medlemmar är en prioritet, och vi uppmuntrar alla som kan ha frågor eller funderingar kring sin insulinpump att konsultera sin läkare och kontakta Medtronic för mer information. Vi kommer att fortsätta att arbeta nära Medtronic samt övervaka de senaste kliniska bevisen för att se till att våra medlemmar med diabetes har fortsatt tillgång till säker och prisvärd vård. ”
Vi skulle vara nyfikna att se några uppgifter om hur ofta människor tar upp produktåterkallningsfrågor i sina täckningsförfrågningar och överklaganden, och vad försäkringsgivarna gör åt det övergripande.
Hur svarar läkare på återkallande av medicinska produkter?
Vi var också nyfikna på hur läkare och diabetesvårdsspecialister kan hantera patienternas oro över produktsäkerhetsfrågor, vi kontaktade flera för att fråga vad de skulle kunna ge någon som står inför dessa bekymmer. Temat är ganska konsekvent: Det är från fall till fall, beroende på vilken produkt eller medicin som är inblandad. Ofta kommer läkare att kontakta företaget direkt för mer information och eventuella behov.
"Vi försöker vara proaktiva och se om det verkligen är en fara som våra patienter skulle drabbas av", säger Dr. Jennifer Dyer, en pediatrisk endokrinolog i Ohio.
”Vi är ganska tålmodiga med (dessa problem) eftersom vi vet att de är maskiner och ibland kan vara opålitliga, så vi lär alltid våra patienter att vara smartare än maskinerna. I vår praxis har vi ett extremt grundligt program baserat på den principen, så tack och lov är våra patienter i allmänhet OK när dessa saker händer. I det senaste fallet bör våra patienter ha det bra enligt våra protokoll, förklarar hon.
I Texas säger endokrinolog och diabetesförfattare Dr Stephen Ponder att han också diskuterar eventuella återkallelser med patienter och låter dem bestämma hur de ska gå vidare. Ibland vill de kontakta ett företag om ett specifikt problem, medan andra patienter är övertygade om att de inte har en funktionsfel och är glada att fortsätta använda den.
"Enligt min erfarenhet är återkallelser helt enkelt en del av livet", sa han. ”Jag vet inte om vi skyndar på produkter för tidigt eller inte. Vi har en mer sofistikerad användarbas inom diabetes nu än någonsin i historien och den användarbasen är sammankopplad via sociala medier. Det gör att produktproblemen kan återkomma med högre och snabbare intensitet än på 70-, 80- eller 90-talet. ”






















.jpg)

